Así funcionan los ensayos clínicos en el desarrollo de una vacuna

Brigadas del Municipio de Quito realizan pruebas PCR a ciudadanos en el sur de la ciudad, el 17 de diciembre de 2020.
Municipio de Quito
Autor:
Actualizada:
Compartir:
Para comprobar que medicamentos y vacunas son seguros y eficaces es necesario que atraviesen por tres fases de verificación científica. Este proceso se conoce como ensayo clínico.
El farmacólogo de la Universidad San Francisco de Quito, Enrique Terán, explica en qué consisten estas tres etapas:
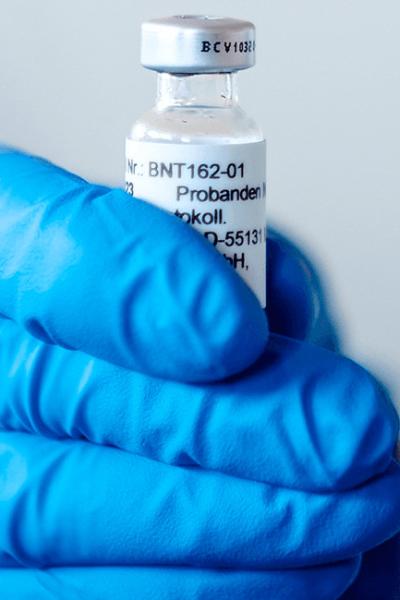
Fase 1
Sirve para descartar la toxicidad del fármaco o de la vacuna y determinar si producen algún daño en las personas. Se aplica en 20 o 30 voluntarios, pues es considerada una etapa riesgosa.
Generalmente, quienes aceptan recibir la dosis obtienen una remuneración económica. Es la fase más complicada porque la seguridad del medicamento es mínima.
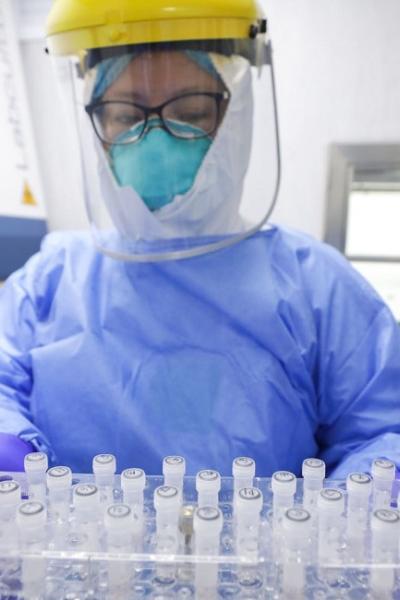
Fase 2
En esta etapa se busca establecer las dosis necesarias para combatir la enfermedad y que la vacuna provoque los efectos que se busca en los pacientes.
En esta etapa, alrededor de 100 personas reciben el medicamento o la vacuna en desarrollo. En esta fase también se pone mucha atención en los efectos secundarios que pueden aparecer.
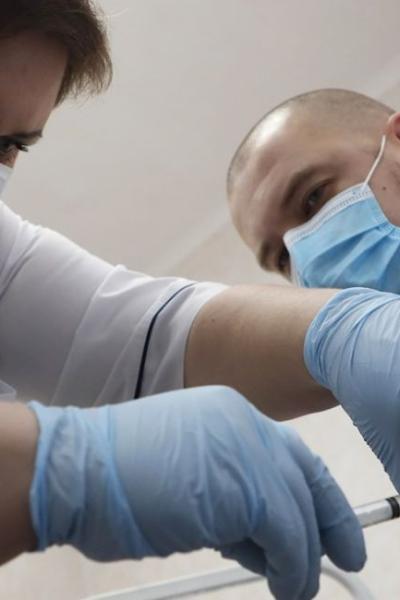
Fase 3
El medicamento o vacuna se aplica a miles de voluntarios. Se trata de la última etapa de prueba antes de que el producto pueda ser aprobado y comercializado.
En esta fase se administra el medicamento a la mitad de los voluntarios, mientras que la otra mitad recibe un placebo. El objetivo es que ningún paciente sepa la sustancia que recibió para que los resultados no sufran alteraciones.
Terán dice que, al finalizar la fase 3, los investigadores dan a conocer el porcentaje de efectividad del fármaco, en función de los resultados que se produzcan en los voluntarios.
En esta tercera fase participarán, a partir de enero de 2021, entre 5.000 y 8.000 voluntarios ecuatorianos que serán parte del ensayo clínico de una de las vacunas chinas contra el Covid-19, según el ministro de Salud, Juan Carlos Zevallos.
Si la vacuna o el medicamento cumple con los requisitos establecidos por las agencias reguladoras, como la Administración de Medicamentos y Alimentos de Estados Unidos (FDA), recibirá la aprobación para ser comercializado.
El profesor de la Universidad Central, Fabricio González, advierte que al concluir la fase 3 no termina el ensayo clínico.
"Los desarrolladores deben realizar un seguimiento para determinar si no hay grandes efectos secundarios con el transcurso del tiempo entre quienes recibieron el producto en desarrollo. Solo así se comprobarán su eficacia y su seguridad", dice.
Este monitoreo -indica- se realiza con un equipo de profesionales que siguen de cerca la evolución de cada paciente para verificar la eficacia del producto.
Requisitos para un ensayo clínico
El Ministerio de Salud cuenta con un reglamento para la realización de ensayos clínicos en Ecuador.
Se trata de un documento de 25 páginas y 96 artículos, en el que se establece que la Agencia Nacional de Regulación, Control y Vigilancia Sanitaria (Arcsa) es el ente regulador de estos procesos.
El documento recoge las obligaciones que deben cumplir las empresas que realizarán el proceso, así como los derechos de quienes participarán.
Entre los principales artículos están:
- La empresa investigadora debe contar con la aprobación de la Agencia Nacional de Regulación, Control y Vigilancia Sanitaria (Arcsa).
- Los ensayos clínicos se realizarán bajo condiciones que aseguren el respeto a los derechos humanos.
- Arcsa realizará inspecciones para garantizar la seguridad de los voluntarios.
- Debe existir un documento de consentimiento informado, firmado por el voluntario.
- Los ensayos clínicos deben contar con un Comité de Ética de Investigación en Seres Humanos para garantizar los derechos de los participantes.
- La empresa investigadora debe reportar inmediatamente si se presentan los efectos adversos.
El ministro de Salud, Juan Carlos Zevallos, dice que los protocolos del ensayo clínico de la vacuna contra el Covid-19 que iniciará en enero de 2021 aún se encuentran en desarrollo.
El proceso tiene que contar con la autorización de la Arcsa.
Escasa participación en ensayos clínicos
Los investigadores Enrique Terán y Fabricio González, junto al exdirector del Instituto Nacional de Higiene Izquieta Pérez, Francisco Hernández, coinciden en que Ecuador ha tenido una escasa participación en ensayos clínicos.
Para Terán, la principal razón es la falta de infraestructura científica que tiene el país para ser parte de estos procesos.
A esto se suman- dice González- las "trabas burocráticas que hacen imposible que una empresa se instale en el país para hacer ensayos clínicos".
Mientras que Hernández dice que "al ser un país pequeño, Ecuador no está en el radar de las grandes empresas científicas que buscan sacar al mercado nuevos medicamentos o vacunas".
Es por eso que califican como positivo el ensayo clínico que una empresa china tiene previsto realizar en el país para buscar la aprobación de una nueva vacuna.
El ministro de Salud, Juan Carlos Zevallos, agrega que el principal objetivo es saber si esa vacuna protege a las personas de las 25 variantes del SARS-CoV-2 que se han identificado en Ecuador.
Zevallos aclara que la empresa "correrá con todos los gastos del estudio" y explica que este ensayo clínico abre la posibilidad para que Ecuador produzca vacunas contra el Covid-19.
Compartir: